Le vieillissement est un processus qui affecte toutes les fonctions du corps humain, et notamment celles du cerveau. Cependant, il est possible de retarder le vieillissement en adaptant son mode de vie (exercice physique, restriction calorique, etc.). Des chercheurs de l’Institut Pasteur et du CNRS ont élucidé les propriétés d’une molécule présente dans le sang dont les mécanismes étaient jusqu’à aujourd’hui inconnus, le GDF11. Ils ont montré, à l’aide d’un modèle murin, que cette molécule pouvait imiter les bénéfices de certaines restrictions caloriques, comportements alimentaires qui ont prouvé par ailleurs leur efficacité sur la réduction des maladies cardiovasculaires, la prévention des cancers et l’augmentation de la neurogenèse dans le cerveau. Les résultats de cette étude ont été publiés le 22 octobre 2019 dans Aging Cell.
Aujourd’hui, il est possible de garder un cerveau en bonne santé longtemps. Depuis 30 ans, il est admis que certaines méthodes de restriction alimentaire, comme le jeûne intermittent, permettent d’améliorer les performances cognitives et allongent l’espérance de vie chez plusieurs espèces. Par ailleurs, il a été prouvé que la restriction calorique (réduction de l’apport calorique de 20 % à 30 % en préservant la qualité nutritive) diminue les risques cardiovasculaires, l’apparition des cancers, tout en augmentant la création de nouveaux neurones dans le cerveau.
Dans une précédente étude sur modèle murin, les scientifiques ont observé que l’injection de sang d’une jeune souris chez une souris âgée permettait le rajeunissement des vaisseaux sanguins, dans le cerveau notamment, et améliorait par conséquent le flux sanguin cérébral tout en stimulant la neurogenèse et la cognition[1]. Les chercheurs de l’unité Perception et Mémoire (Institut Pasteur/CNRS) ont émis l’hypothèse que la restriction calorique et la composition du sang jeune, menant tous deux au rajeunissement des organes, devaient partager certains mécanismes.
Ils ont ainsi porté leur intérêt sur la molécule GDF11, une molécule appartenant à la famille de protéines GDF (Growth Differentiation Factor) et impliquée dans le développement embryonnaire. Cette molécule était déjà connue des scientifiques pour ses propriétés rajeunissantes dans le cerveau âgé. « En injectant cette molécule sur des modèles murins âgés, nous avons remarqué une augmentation de la neurogenèse et du modelage des vaisseaux sanguins » explique Lida Katsimpardi, chercheuse au sein de l’unité Perception et Mémoire et première auteure de l'étude. Par ailleurs, les chercheurs ont également observé que les souris auxquelles la molécule GDF11 avait été administrée perdaient du poids, sans modification de leur appétit. Un constat qui les a conduits à penser que c’était bien cette molécule qui faisait le lien entre restriction calorique et pouvoir du sang jeune de régénération.
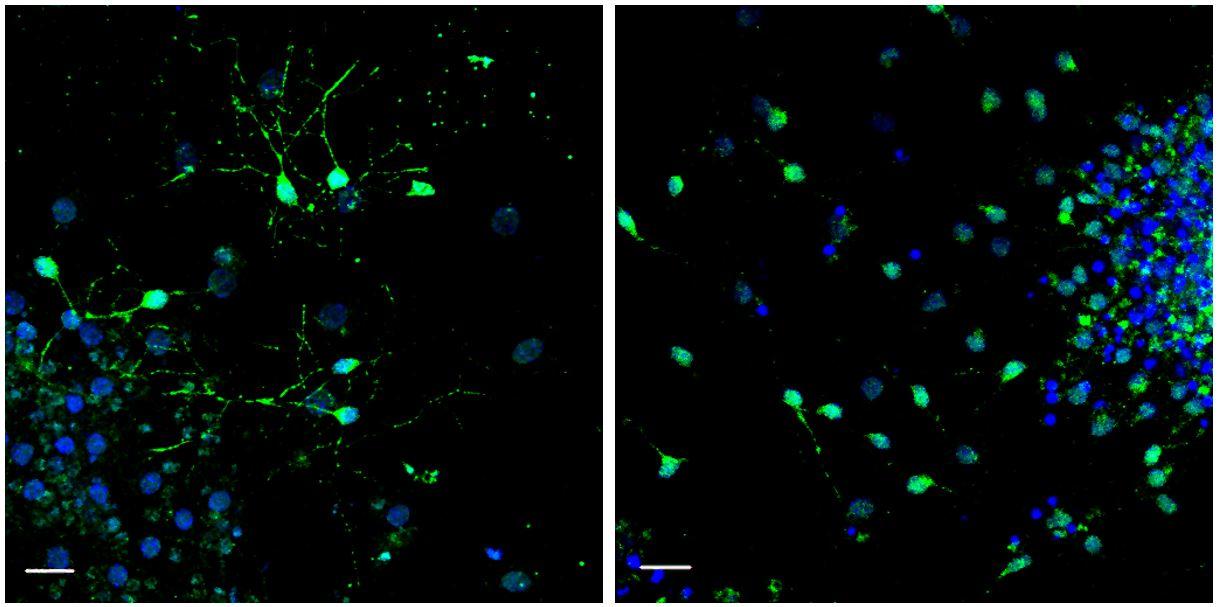
A gauche : neurogenèse induite par supplémentation de GDF11 dans le sang âgé. A droite : absence de neurogenèse avec le sang âgé. © Institut Pasteur
La deuxième étape a été de confirmer cette hypothèse en étudiant une deuxième molécule, l’adiponectine, une hormone sécrétée par le tissu adipeux et responsable d’une perte de poids sans modification de l’appétit. Chez les animaux ayant subi une restriction calorique, les niveaux sanguins de cette hormone sont élevés. « Chez les animaux ayant reçu GDF11, nous avons également observé des niveaux élevés d’adiponectine, souligne Lida Katsimpardi, ce qui montre que l’administration de GDF11 entraîne des modifications métaboliques similaires à celles induites par la restriction calorique. »
Jusqu’ici, le rôle de GDF11 dans le vieillissement restait controversé et ses mécanismes, largement inconnus. Les résultats de cette étude montrent que GDF11, induisant des phénomènes semblables à ceux d’une restriction calorique contrôlée par la stimulation directe d’adiponectine, permet la formation de nouveaux neurones dans le cerveau. « Ces résultats sont encourageants pour envisager une utilisation thérapeutique de GDF11 dans certaines maladies métaboliques comme l’obésité ou les maladies neurodégénératives » conclut Pierre-Marie Lledo, chercheur CNRS, responsable du laboratoire Perception et Mémoire à l’Institut Pasteur et dernier auteur de l’étude.
[1] (Katsimpardi et al, Science, 2014)
Source
Systemic GDF11 stimulates the secretion of adiponectin and induces a calorie restriction-like phenotype in aged mice, Aging Cell, 22 octobre 2019
Lida Katsimpardi1,2,§, Nicolas Kuperwasser3, Claire Camus1,2, Carine Moigneu1,2, Aurélie Chiche5, Virginie Tolle4, Han Li5, Erzsebet Kokovay6 and Pierre-Marie Lledo1,2
1 Perception and Memory Lab, Neuroscience Department, Institut Pasteur, F-75015 Paris, France
2 Centre National de la Recherche Scientifique, Unité Mixte de Recherche 3571, F-75015 Paris, France
3 Institut National de la Santé et de la Recherche Médicale (INSERM) U1151, Institut Necker Enfants Malades (INEM), Dept. of Cell growth and signaling, Université Paris Descartes -Sorbonne – Paris Cité, 75014 Paris, France
4 Centre de Psychiatrie et Neurosciences, UMR-S 894 INSERM, Université Paris Descartes Sorbonne Paris Cité, Paris, France
5 Cellular Plasticity & Disease Modelling, Dept. of Developmental & Stem Cell Biology, CNRS UMR 3738, Institut Pasteur, F-75015 Paris, France
6 Cell Systems and Anatomy, Brashop Institute for Longevity and Aging Studies, University of Texas Health Science Center at San Antonio, San Antonio, TX, USA
§ lead contact