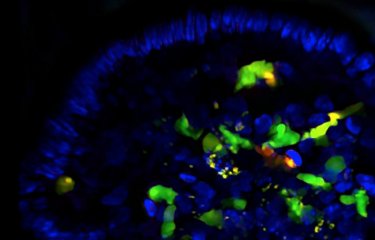
Des chercheurs ont évalué l’influence des contractions mécaniques de l’intestin sur l’invasion de deux agents pathogènes, l’un responsable de l’amibiase et l’autre de la shigellose. Pour y parvenir, les travaux s’appuient sur l’imagerie computationnelle 3D et la technologie organ-on-chip. Grâce à cette technologie, les chercheurs ont reproduit fidèlement les caractéristiques physiologiques de l’intestin sur une puce pas plus grande que quelques centimètres.
Les forces physiques sont essentielles aux fonctions biologiques, mais leurs influences au niveau des tissus ne sont pas encore comprises. L’intestin est soumis à un stress mécanique constant causé par le péristaltisme, terme qui désigne l’ensemble des contractions musculaires permettant la progression d’un contenu à l’intérieur d'un organe creux.
A l’Institut Pasteur, Nathalie Sauvonnet est responsable du groupe Trafic intracellulaire et homéostasie tissulaire. Elisabeth Labruyère, quant à elle, est chercheuse au sein de l’unité d’Analyse d’images biologiques, dirigée par Jean-Christophe Olivo-Marin. Ces deux chercheuses ont croisé les compétences de leurs unités pour évaluer l’influence du péristaltisme sur deux agents pathogènes de l’intestin.
- L’amibe Entamoeba histolytica (responsable de l’amibiase)
L’amibiase est provoquée par l’amibe Entamoeba histolytica, parasite spécifique de l’Homme. Si l’infection reste généralement asymptomatique, le parasite peut cependant, en traversant la muqueuse de l’intestin, provoquer des diarrhées douloureuses et sanglantes et des ulcères. Et, dans les formes plus sévères, entraîner des abcès au niveau du foie, des poumons et du cerveau.
En savoir plus sur l’amibiase
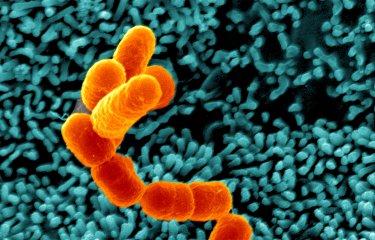
- La bactérie Shigella flexneri (responsable de la shigellose)
La shigellose est provoquée par une bactérie nommée Shigella, un clone spécialisé de Escherichia coli. Elle contient un plasmide de virulence qui lui permet d’envahir les cellules épithéliales intestinales puis les muqueuses. Ce processus aboutit à une intense inflammation qui s’accompagne d’une sévère destruction tissulaire.
En savoir plus sur la shigellose
Gut-on-chip : reproduire un intestin sur une puce
La technologie des organes sur puce (organ-on-chip) consiste à reproduire fidèlement les caractéristiques physiologiques d’un organe sur une cartouche pas plus grande qu’une clé USB (voir encadré plus bas : « Organ-on-chip : une technologie vouée à se développer »). « Pour nos travaux sur le péristaltisme, la technologie organ-on-chip nous permis de recréer une sorte de mini-intestin fonctionnel – ou gut-on-chip – », explique Nathalie Sauvonnet. « Les deux pathogènes de l’étude provoquent des maladies seulement chez l’homme, et aucun modèle animal reproduit bien ces maladies. » Les scientifiques y ont placé les cellules intestinales étudiées, reproduisant ainsi les conditions mécaniques d’un intestin grâce aux technologies implantées dans la puce.
Le gut-on-chip et l’imagerie 3D pour comprendre les pouvoirs infectieux
Les équipes de Nathalie Sauvonnet et Elisabeth Labruyère ont utilisé le gut-on-chip et l’imagerie computationnelle pour étudier le comportement de ces deux pathogènes. Après avoir infecté l’appareil avec l’un des deux microbes, son comportement est imagé en temps réel et en 3D. Cependant, les microscopes confocaux ne sont pas assez rapides pour imager le mouvement péristaltique dans la puce en 3D. « Afin d’observer l'invasion des pathogènes en 3D, il a fallu développer une méthode de post-traitement qui reconstruit des vidéos 3D en combinant des acquisitions 2D prises à l’aide d’un microscope programmable. Ceci nous a permis d’étudier l’infection de manière quantitative, par exemple en utilisant des algorithmes pour mesurer le moment d’activation de certains gènes virulents », explique Aleix Boquet-Pujadas, auteur principal de l’étude. Avec les données prélevées en temps réel, les auteurs ont ensuite étudié le rôle du stress mécanique dans l’infection grâce à une méthode de calcul permettant de mesurer la tension locale du tissu sous péristaltisme. La combinaison de ces approches interdisciplinaires alliant l’ingénierie, la biologie, la physique et l’analyse quantitative, a ainsi permis d’obtenir une image plus complète des mécanismes d’invasion des agents pathogènes.
Cette étude montre notamment que le péristaltisme :
- facilite la pénétration du parasite E. histolytica puis la destruction du tissu intestinal ;
- accélère la colonisation par les bactéries S. flexneri et déclenche chez elles l’expression de gènes virulents ;
Ces deux phénomènes sont amplifiés dans les zones du tissu soumises à une plus forte contrainte mécanique locale.
« Notre travail souligne le rôle fondamental des contraintes physiques lors des interactions hôte-pathogène et fournit un nouveau cadre qui ouvre la porte à des études mécanobiologiques sur les tissus déformables », souligne Elisabeth Labruyère à propos de l’étude parue le 21 octobre 2022.
Organ-on-chip : une technologie vouée à se développer
A l’Institut Pasteur, la plateforme Biomatériaux et microfluidique (page en anglais) déploie la technologie d’organ-on-chip développée par l’entreprise de biotechnologie Emulate® (Boston, Etats-Unis). « Cette technologie consiste à reproduire fidèlement les caractéristiques physiologiques de différents tissus ou organes comme les intestins, les alvéoles pulmonaires, le foie…, sur une puce microfluidique », explique Samy Gobaa, responsable de la plateforme à l’Institut Pasteur. Utiliser les organes-sur-puce permet d’agir sur les trois leviers qui visent à éviter l’expérimentation animale ou du moins à améliorer (Refine), réduire (Reduce) et remplacer (Replace) l’utilisation d’animaux en recherche dès que cela est possible (règle dite des 3R), un engagement pour l’Institut Pasteur.
Depuis 2019, ce centre d’organ-on-chip de l’Institut Pasteur a ouvert une série d’appels à projets afin de faciliter l’accès à cette technologie.
La plateforme Biomatériaux et microfluidique est soutenue par l'institut Carnot Pasteur Microbes & Santé (Pasteur MS).
Voir aussi : La technologie des « organes-sur-puce » au service de la recherche biomédicale