Les cellules des rares individus contrôlant naturellement l’infection au VIH sont étudiées depuis près de 15 ans afin de décrypter leurs particularités. Des chercheurs de l’Institut Pasteur, grâce aux cohortes ANRS CO21 CODEX et CO6 PRIMO, ont décrit les caractéristiques des cellules immunitaires CD8 de sujets dits « contrôleurs du VIH ». Le pouvoir antiviral si particulier de ces cellules est dû à un programme métabolique optimal qui leur permet de persister et réagir efficacement contre les cellules infectées. Les chercheurs sont parvenus à reprogrammer ex vivo des cellules d’individus infectés non-contrôleurs leur conférant le pouvoir antiviral des cellules des contrôleurs. Ces résultats sont publiés le 12 juillet 2019 dans la revue Nature Metabolism.
Certaines personnes réussissent à contrôler naturellement le VIH, sans traitement. Chez ces individus, très rares, (moins de 1% des personnes vivant avec le VIH), on ne détecte pas de multiplication du virus dans leur sang, en l’absence de traitement pendant plus de 10 ans d’infection. En 2007, les chercheurs de l’Institut Pasteur décrivaient comment leurs lymphocytes CD8 ont une activité antivirale extraordinaire. En effet, les CD8 de contrôleurs parviennent à détruire rapidement les cellules CD4 infectées, contrairement aux cellules CD8 de non-contrôleurs.
Les chercheurs de l’unité VIH, inflammation et persistance à l’Institut Pasteur ont donc poursuivi leurs recherches pour connaitre les caractéristiques précises de ces cellules dans le but de les conférer aux cellules des sujets non-contrôleurs.
D’apparence extérieure les cellules CD8, dites « mémoires », des contrôleurs sont identiques à celles des non-contrôleurs mais les chercheurs ont montré qu’elles ont un programme moléculaire différent. Ils ont décrit que chez les contrôleurs les cellules CD8 anti VIH ont un grand potentiel antiviral mais aussi qu’elles sont programmées pour survivre ; tandis que le programme des cellules des non-contrôleurs les prédisposent à l’épuisement et à la mort cellulaire.
Pour mener leurs activités les cellules CD8 des contrôleurs utilisent des ressources métaboliques variées et en particulier elles fonctionnent sur l’apport énergétique de leurs mitochondries1, bien adapté pour permettre la survie de la cellule dans des conditions de stress. A l’inverse, les cellules des non-contrôleurs sont dépendantes d’une seule source d’énergie (le glucose) et leurs mitochondries montrent une activité limitée. « Nous avons donc identifié que l’activité antivirale des CD8 des contrôleurs est associée à la mise en place d’un programme optimal qui leur confère une plasticité dans l’utilisation des ressources énergétiques de la cellule », explique Asier Saez-Cirion, coordinateur de l’étude, chercheur au sein de l’unité VIH, inflammation et persistance à l’Institut Pasteur.
Les scientifiques sont alors parvenus dans le laboratoire à stimuler l’activité des mitochondries chez les cellules CD8 anti VIH des non-contrôleurs. Grâce à une substance sécrétée par le système immunitaire, appelée interleukine 15 (IL-15), les cellules de non-contrôleurs récupèrent leur activité mitochondriale et augmentent leur potentiel anti-VIH. Les cellules CD8 reprogrammées des non-contrôleurs acquièrent ainsi une capacité à détruire les cellules CD4 infectées qui ressemble à celle des cellules des contrôleurs.
« Nos travaux montrent que même si les cellules CD8 anti VIH des non-contrôleurs sont relativement inefficaces, les différences avec les cellules de contrôleurs ne sont pas insurmontables », conclut Asier Saez-Cirion.
La reprogrammation métabolique des cellules immunitaires est une stratégie déjà actuellement en phase d’essais cliniques pour le traitement des cancers. Les chercheurs espèrent pouvoir tester ces stratégies in vivo prochainement pour ces facultés anti-VIH.
Ces travaux ont été financés par l’Institut Pasteur, ainsi que par l’ANRS, MSDAVENIR, l’Union Européenne (Horizon 2020) et Sidaction.
1 Mitochondrie : organite situé à l’intérieur de la cellule qui fournit l’énergie nécessaire au bon fonctionnement cellulaire.
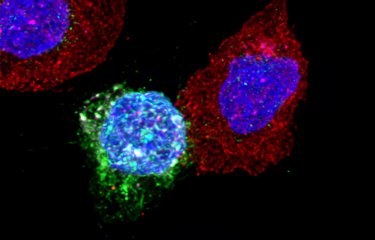
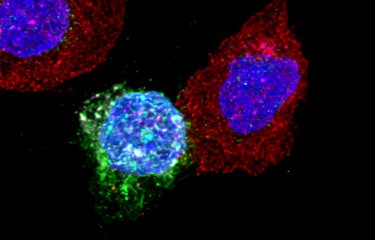
Légende : Lymphocytes CD8 (rouge) de patients contrôleurs en contact avec des cellules CD4 (vert) infectées par le VIH. Les noyaux des cellules sont en bleu. En rose une molécule cytotoxique sécrétée par les CD8 pour détruire les CD4.
Source
Metabolic plasticity of HIV-specific CD8+ T-cells is associated with enhanced antiviral potential and natural control of HIV-1 infection, Nature Metabolism, 12 juillet 2019
Mathieu Angin1, Stevenn Volant2, Caroline Passaes1, Camille Lecuroux3, Valérie Monceaux1, Marie-Agnes Dillies2, José Carlos Valle Casuso1, Gianfranco Pancino1, Bruno Vaslin3, Roger Le Grand3, Laurence Weiss4,5, Cecile Goujard6, Laurence Meyer7, Faroudy Boufassa7, Michaela Müller-Trutwin1, Olivier Lambotte3,6, and Asier Sáez-Cirión1
1 Institut Pasteur, Unité HIV Inflammation et Persistance, Paris, France
2 Institut Pasteur, Hub Bioinformatique et Biostatistique – C3BI, USR 3756 IP CNRS – Paris, France
3 CEA, Université Paris Sud, INSERM U1184, Immunology of Viral Infections and Autoimmune Diseases (IMVA), IDMIT Department / IBFJ, 92265 Fontenay-aux-Roses, France
4 Assistance Publique Hôpitaux de Paris, Hôpital Européen Georges Pompidou, Paris, France
5 Université Paris Descartes, Sorbonne Paris Cité, Paris, France
6 Assistance Publique Hôpitaux de Paris, Hôpital Bicêtre, Service de Médecine Interne et Immunologie clinique, 94275 Le Kremlin-Bicêtre, France
7 INSERM U1018, Centre de recherche en Epidémiologie et Santé des Populations, Université Paris Sud, Le Kremlin Bicêtre, France