Les cancers d’origine infectieuse

Plus d’un cancer sur six dans le monde est d’origine infectieuse. Au total, chaque année 2,2 millions de nouveaux cas de cancers découleraient d’une infection par un agent pathogène. Huit virus, une bactérie et trois parasites ont en effet été classés agents cancérigènes du groupe 1 (agents cancérigènes « certains ») par le Centre international de recherche sur le cancer, une division de l’Organisation mondiale de la santé.
Parmi eux, le virus de l’hépatite B et celui de l’hépatite C peuvent conduire à des infections chroniques et au cancer du foie, et sont responsables de plus d’un million de décès annuels. La bactérie Helicobacter pylori est, elle, en cause dans la majorité des cas de cancer de l’estomac, seconde cause de mortalité par cancer dans le monde. L’infection par certains papillomavirus est à l’origine des cancers du col de l’utérus - quatrième cause de mortalité par cancer chez les femmes. Le virus du sida est également classé cancérigène car l’immunodéficience qu’il déclenche conduit à un risque accru de cancers.
Un parasite, premier suspect historique
Les suspicions autour de l’implication d’agents infectieux dans des cancers commencèrent dès la fin du XIXe siècle et concernèrent alors des parasites, notamment l’agent de la bilharzioze, qui sévit dans les régions tropicales et subtropicales. L’infection chronique par ce parasite peut conduire au cancer de la vessie, mais il fallut 50 ans pour que les preuves de son implication émergent. Aujourd’hui, il est établi que trois parasites peuvent être à l’origine de cancers : celui de la bilharzioze donc, et deux autres vers parasites, l’un endémique dans certains pays d’Asie du Sud-Est (Thaïlande, Laos, Vietnam, Cambodge…) et l’autre en Extrême-Orient, tous deux associés à des cancers de la vésicule et des voies biliaires.
Epstein-Barr : le premier virus impliqué
La deuxième grande étape dans l’histoire des cancers d’origine infectieuse débute en 1958 : un chirurgien britannique, Denis Burkitt, décrit un lymphome touchant les enfants en Afrique Equatoriale (nommé depuis « lymphome de Burkitt ») et émet l’hypothèse d’une origine infectieuse de ce cancer. En 1964, son compatriote Michael Epstein découvre des particules virales dans des cellules cultivées à partir de ces lymphomes. Il fut démontré au début des années 70 que le virus « d’Epstein-Barr » était bien à l’origine du lymphome de Burkitt. Présent chez la majorité des individus, heureusement le plus souvent sans conséquences, ce virus est également associé à un cancer du nasopharynx. C’est le tout premier virus qui fut formellement impliqué dans la survenue de cancers humains.
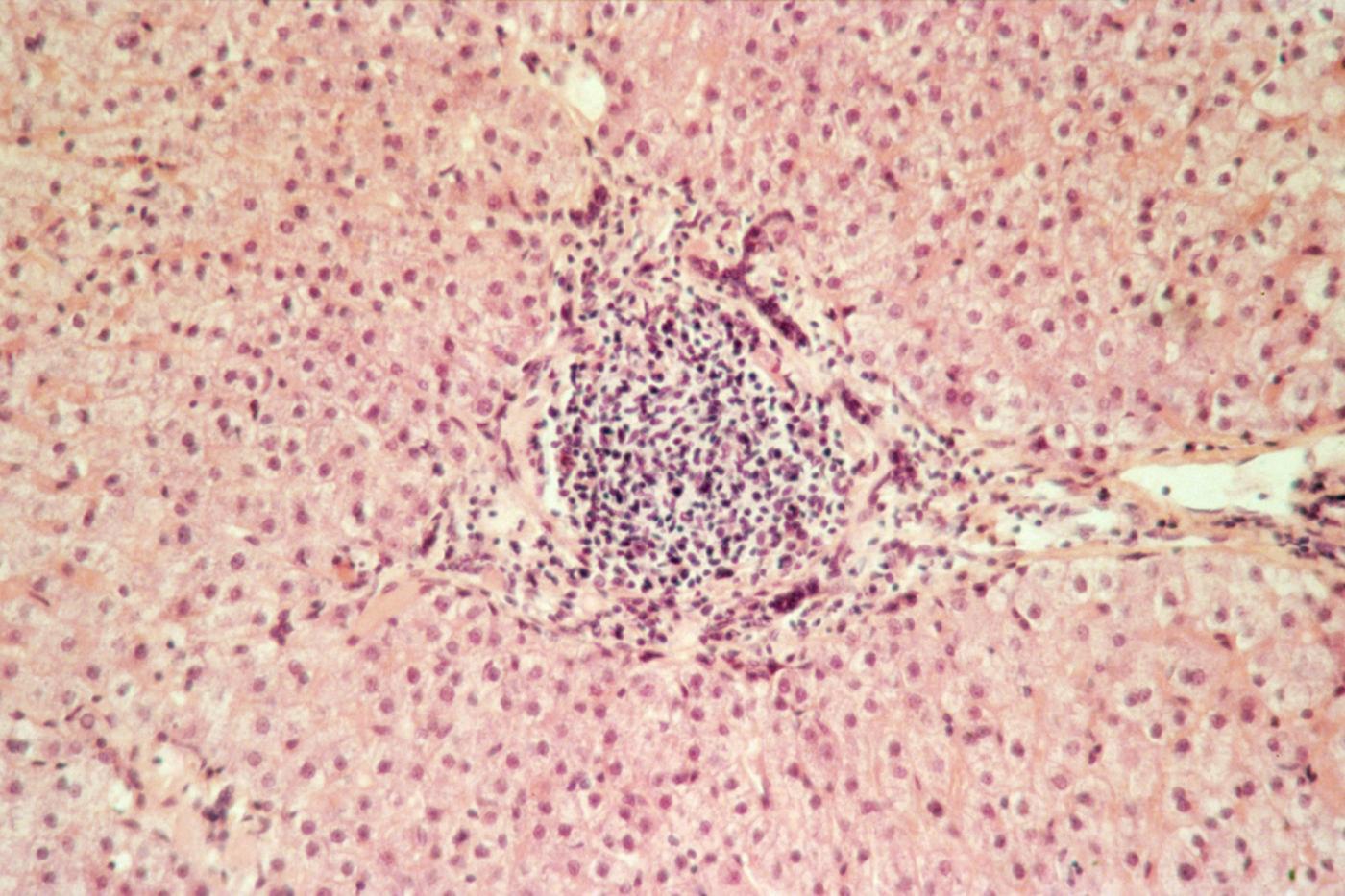
Ci-dessus : coupe histologique de foie de patient atteint d'hépatite C. L'hépatite C chronique peut être à l'origine de cirrhose et cancer du foie. © Institut Pasteur
Nouveaux traitements et biomarqueurs
700 000 nouveaux cas de cancer du foie surviennent chaque année dans le monde. « Si la majorité de ces cancers sont d’origine infectieuse, il faut souligner que dans les pays industrialisés, leur cause première est la cirrhose alcoolique » remarque le Pr Stanislas Pol, responsable de l’unité d'Immunobiologie des cellules dendritiques et du Centre de Recherche Translationnelle à l’Institut Pasteur, et chef du département d’hépatologie de l’hôpital Cochin. Quelle que soit leur origine, ces cancers sont difficiles à traiter : le cancer du foie est devenu la première cause de transplantation hépatique en France. La recherche de traitements plus efficaces est nécessaire. « Avec l’hôpital de La Pitié Salpétrière, nous menons actuellement un essai d’immunothérapie chez des patients atteints de cancers du foie, avec une molécule nommée sitagliptine, en vue notamment de réduire la taille des tumeurs » précise Stanislas Pol, déjà à l’origine d’importantes avancées dans le traitement des hépatites virales.
Autre enjeu : le dépistage précoce du cancer. Pascal Pineau, de l’unité Organisation nucléaire et oncogenèse, dirigée par Anne Dejean, étudie les particularités des cancers du foie selon les régions du monde, à travers les dérèglements génétiques induits par les hépatites virales dans les hépatocytes de sujets cancéreux. Parmi ses objectifs : identifier des biomarqueurs des phases précoces de ces cancers. Il analyse actuellement biopsies du foie et prélèvements sanguins de centaines de patients africains, avec les instituts membres du Réseau international des instituts Pasteur (Centre Pasteur du Cameroun et Institut Pasteur de Bangui en République Centrafricaine). « Mais le cancer du foie a une grande hétérogénéité géographique », souligne le chercheur. « Il nous faudra trouver un panel de marqueurs. Nous ne sommes qu’au début de cette quête. »
Des cancers potentiellement évitables
Dans les années 70, l’effet potentiellement cancérigène de plusieurs autres virus fut établi : le virus de l’hépatite B, suspecté dès les années 50 d’être associé au cancer du foie, un rétrovirus associé à une forme rare de leucémie (HTLV-1), ou encore plusieurs types de papillomavirus en cause dans le cancer du col de l’utérus. Puis vint la preuve de l’implication de la bactérie Helicobacter pylori, la seule bactérie - même si d’autres sont actuellement suspectées - aujourd’hui classée agent cancérigène du groupe 1, depuis 1994. Cette même année fut découvert un autre virus cancérigène, l’herpèsvirus 8 en cause dans le sarcome de Kaposi, rendu tristement célèbre par l’épidémie de sida mais qui touche aussi des personnes séronégatives en Afrique. Le tout dernier agent classé dans le fameux groupe 1 est un virus identifié en 2008 et relativement rare : le « polyomavirus » de Merkel, associé à un cancer très agressif de la peau.
Qu’ont en commun les cancers associés à tous ces pathogènes ? Ils sont évitables si l’on parvient à empêcher l’infection en cause, ou à la traiter à temps. Un immense pas fut franchi en ce sens dans les années 80, face à l’hépatite B et au cancer du foie.

Prévenir ou traiter l’infection, c’est faire disparaître le risque de cancer associé.
Quelle est la place des cancers d’origine infectieuse dans le monde ?
30 à 50% des 14 millions de cancers qui surviennent chaque année dans le monde sont évitables. Il y a le tabac, l’alcool, les pesticides, divers autres produits chimiques toxiques… et des agents infectieux, impliqués dans plus de 15% des cas de cancers, avec de grandes disparités selon les régions du monde. Dans les pays occidentaux, on estime que moins de 10% des cancers sont d’origine infectieuse - ce qui est déjà beaucoup –, un chiffre qui atteint 30% dans les pays en développement. Si l’on prend l’exemple de l’Inde, où vit près d’une personne sur 5 dans le monde, elle concentre un quart des cas mondiaux de cancers du col de l’utérus. Une autre caractéristique des cancers d’origine infectieuse est qu’ils surviennent généralement plus tôt dans la vie que les autres. Pour un certain nombre d’agents pathogènes cancérigènes, le facteur de risque d’acquérir une tumeur, c’est le fait d’être infecté très jeune, voire bébé. C’est le cas de l’hépatite B et du cancer du foie, qui peut survenir chez de jeunes adultes.
Comment ces agents pathogènes provoquent-ils des cancers ?
Il y a différents cas de figure. Plusieurs types de papillomavirus, l’HTLV-1, le virus Epstein-Barr ou l’herspèsvirus 8 sont des oncogènes « directs » – ils produisent par exemple des protéines qui conduisent à la transformation des cellules. Et puis il y a les oncogènes indirects : soit par l’inflammation chronique qu’ils induisent, elle-même à l’origine de la cancérisation – comme les virus des hépatites B et C, la bactérie H. pylori et les parasites cancérigènes ; soit via l’immunosuppression : c’est le cas du virus du sida. La plupart des cancers liés à ce virus sont en fait déclenchés par des virus oncogènes directs comme le virus d’Epstein-Barr, l’herspèsvirus 8 ou des papillomavirus, contre lesquels l’organisme ne peut plus se défendre.
L’infection par un agent cancérigène ne conduit pas systématiquement au cancer ?
Loin de là. Les cancers d’origine infectieuse surviennent chez un certain pourcentage seulement de personnes infectées. Le cas extrême, c’est le virus d’Epstein-Barr : la majorité des gens dans le monde est infectée par ce virus et quelques centaines de milliers d’entre eux seulement vont développer une tumeur associée. Ce virus est donc très fréquent mais donne rarement des cancers. Le risque est variable selon les agents infectieux cancérigènes, mais la part des gens infectés qui développent des cancers est relativement faible. Ce qui veut dire que pour qu’un cancer survienne, l’agent infectieux est nécessaire mais pas suffisant. Cela implique qu’il y ait des co-facteurs. c’est-à-dire d’autres facteurs de risque qui se sur-ajoutent.
Comment la connaissance de l’agent infectieux en cause permet-elle de mieux combattre les cancers ?
Cela permet d’étudier les mécanismes impliqués, de mieux les comprendre, et d’identifier des cibles moléculaires sur lesquelles on peut agir. En pratique, le grand progrès, c’est la vaccination, aujourd’hui possible contre l’hépatite B et les papillomavirus. Prévenir ou traiter l’infection, c’est faire disparaître le risque de cancer associé. Au-delà de la vaccination, d’autres moyens de prévention existent. Prenons l’HTLV-1, un virus très étudié dans mon laboratoire : il est associé à une leucémie extrêmement sévère, avec une moyenne de survie de 6 mois pour les formes aiguës, qui se développe chez ceux qui ont acquis le virus très tôt. Dans des pays où il est endémique et à bon niveau socio-économique - les Antilles, la Guyane, le Brésil ou le Japon par exemple -, le dépistage des femmes enceintes a été instauré. Chez celles qui sont infectées, on préconise d’éviter l’allaitement. Cela permet ainsi d’éviter le développement d’un des pires cancers qui soient.
Le premier vaccin anti-cancer

En 1981, une étude menée à Taiwan, en Chine, où la prévalence de l’hépatite B était alors considérable, montrait que les porteurs de ce virus (transmis le plus souvent de la mère à l’enfant, mais aussi par voies sanguine ou sexuelle) avaient 200 fois plus de risque que les autres de développer un cancer du foie. Un tournant majeur s’amorçait alors : un vaccin contre l’hépatite B, conçu à l’Institut Pasteur (voir encadré ci-dessous), facilement productible à l’échelle industrielle allait voir le jour en 1985. Généralisée dans de nombreux pays du monde, la vaccination allait permettre de réduire drastiquement l’incidence de l’infection et de ses complications, cirrhose et cancer du foie. Des dizaines de millions de personnes ont aujourd’hui été vaccinées dans le monde, et des millions de cancers évités. Le vaccin contre l’hépatite B fut ainsi le premier vaccin capable de prévenir un cancer.
Hépatite B : du vaccin préventif au vaccin curatif
L’actuel vaccin préventif contre l’hépatite B fut mis au point à l’Institut Pasteur, dans l’équipe du Professeur Pierre Tiollais. Disponible dès 1985, ce vaccin efficace à plus de 95% est aujourd’hui utilisé en vaccination systématique chez les nourrissons ou les adolescents dans quelque 200 pays. Selon l’Organisation mondiale de la santé, « plus d’un milliard de doses de vaccin contre l’hépatite B ont été administrées dans le monde. Dans nombre de pays, où 8 à 15% des enfants devenaient auparavant des porteurs chroniques, la vaccination a permis de ramener le taux d’infection chronique à moins de 1% parmi les enfants vaccinés. »

Reste qu’aujourd’hui 250 millions d’individus dans le monde sont déjà porteurs chroniques du virus. « Il s’agit d’un enjeu de santé publique considérable » souligne Maryline Bourgine, dans l’unité de Virologie moléculaire et vaccinologie de l’Institut Pasteur, dirigée par Pierre Charneau. « Nous travaillons à développer un candidat-vaccin thérapeutique pour ces porteurs chroniques*. Le principe est d’amener le patient à faire lui-même sa propre réaction immunitaire contre le virus pour l’éliminer. Nous espérons beaucoup de cette stratégie car, actuellement, les plus performants des antiviraux ne permettent pas de faire disparaître le virus du foie des porteurs chroniques. Nous construisons actuellement plusieurs candidats-vaccins, basés sur une technologie innovante mise au point dans ce laboratoire. Les premiers résultats des tests d’efficacité sont attendus dans les mois à venir.»
*Dans le cadre du Grand Programme Fédérateur "Vaccinologie" de l’Institut Pasteur.
Un deuxième vaccin anti-cancer
Une vingtaine d’années plus tard, en 2007, un deuxième « vaccin anti-cancer » était disponible : dirigé contre les types de papillomavirus les plus fortement impliqués dans le cancer du col de l’utérus, il permet d’éviter dans plus de 60% des cas ce cancer, qui tue plus d’un millier de femmes chaque année en France et constitue le deuxième cancer de la femme dans le monde.

Les papillomavirus impliqués dans les cancers génitaux se transmettent par voie sexuelle, deux d’entre eux (HPV 16 et HPV 18) – « couverts » par les deux vaccins commercialisés - étant à eux seuls responsables de 70% de ces cancers. Ils sont particulièrement courants et la vaccination en France est recommandée chez les filles avant qu'elles soient sexuellement actives, entre 11 et 14 ans, avec un rattrapage possible jusqu’à 20 ans. L’impact de cette vaccination est étudié de près (voir encadré ci-dessous).
Cancer du col de l’utérus : étudier l’impact de la vaccination
Une vingtaine de papillomavirus sont considérés à haut risque car ils peuvent être à l’origine des cancers génitaux. Ces virus sexuellement transmissibles provoquent des lésions bénignes comme des verrues génitales ou des lésions malignes pouvant évoluer – en 15 à 20 ans - en cancer du col de l'utérus. Depuis 2007, les jeunes filles peuvent être vaccinées contre les deux types de papillomavirus majoritairement impliqués dans ce cancer.

L’unité de Pharmacoépidémiologie et maladies infectieuses de l’Institut Pasteur, dirigée par Didier Guillemot, mène une étude chez 1000 jeunes femmes participant à une cohorte d'étudiants pour évaluer l’impact de la vaccination sur la circulation de ces différents virus dans la population. Jusqu’à quel point la vaccination va-t-elle faire baisser la fréquence des deux principaux virus (HPV16 et HPV18) chez les jeunes femmes ? Si elle conduit à leur diminution, d’autres papillomavirus plus rares aujourd’hui ne vont-ils pas prendre le dessus ? Cette étude post-vaccinale apportera des réponses importantes pour anticiper l’effet de la vaccination et proposer des actions de santé publique adaptées.
Traiter pour éliminer l’agent cancérigène
Les deux vaccins cités sont aujourd’hui les seuls permettant de prévenir des cancers. En l’absence de prévention vaccinale, l’alternative pour éviter des cancers d’origine infectieuse consiste à traiter l’infection suffisamment précocement (sachant que plusieurs années s’écoulent –une dizaine au minimum, entre l’acquisition d’un agent pathogène et la survenue d’un cancer).
Citons quelques exemples : une antibiothérapie permet aujourd’hui d’éradiquer la bactérie Helicobacter pylori – qui infecte la moitié de la population mondiale, à risque de cancer de l’estomac. La dernière génération de traitements contre le virus de l’hépatite C élimine définitivement le virus chez ses porteurs chroniques – ils sont des millions dans le monde (voir encadré ci-dessous).
Un test de diagnostic rapide
On estime que 150 millions de personnes dans le monde sont chroniquement infectées par le virus de l’hépatite C. « La plupart ne connaissent pas leur statut », souligne Darragh Duffy, de l’unité d'Immunobiologie des cellules dendritiques à l’Institut Pasteur. Ce chercheur a participé à un programme européen de 3 ans* qui a abouti à un test de diagnostic mobile et rapide du virus. « Entre le temps de transport des échantillons de patients vers un laboratoire et les méthodes d’analyse classiques, il faut souvent une à deux semaines pour le diagnostic. Le test que nous avons élaboré avec la société Epistem est utilisable au chevet du malade et donne le résultat en une heure. Il permettrait ainsi d’identifier facilement les personnes à traiter, car des médicaments très efficaces existent aujourd’hui. Nous le présentons actuellement à des ONG médicales humanitaires, en première ligne sur le terrain ». Si leur généralisation dans les pays en développement est encore limitée par leur coût élevé, ils offrent la perspective de prévenir à l’avenir des centaines de milliers de cas de cancer du foie...
*PoC HCV, coordonné par Matthew Albert, ancien responsable de l’unité d'immunobiologie des cellules dendritiques à l’Institut Pasteur, sous l’égide de l’Inserm.

La recherche a donc permis des avancées considérables face à plusieurs cancers d’origine infectieuse, mais il reste encore beaucoup à faire. Pas moins de 250 millions de personnes dans le monde sont déjà chroniquement infectées par le virus de l’hépatite B et là aucun traitement ne permet d’éliminer le virus de leur organisme…
L’éradication de la bactérie H. pylori par les antibiotiques, belle prévention du cancer de l’estomac, est sérieusement menacée par le développement de l’antibiorésistance (voir encadré ci-dessous)… Les solutions viendront des réponses aux nombreuses questions (quels sont les mécanismes intimes par lesquels ces agents infectieux peuvent induire des cancers ? Comment notre organisme réagit-il face à ces pathogènes ? Pourquoi certaines personnes infectées développent-elles des cancers et pas d’autres ? …) à l’étude dans les laboratoires.
Des cibles thérapeutiques aux marqueurs du cancer de l’estomac
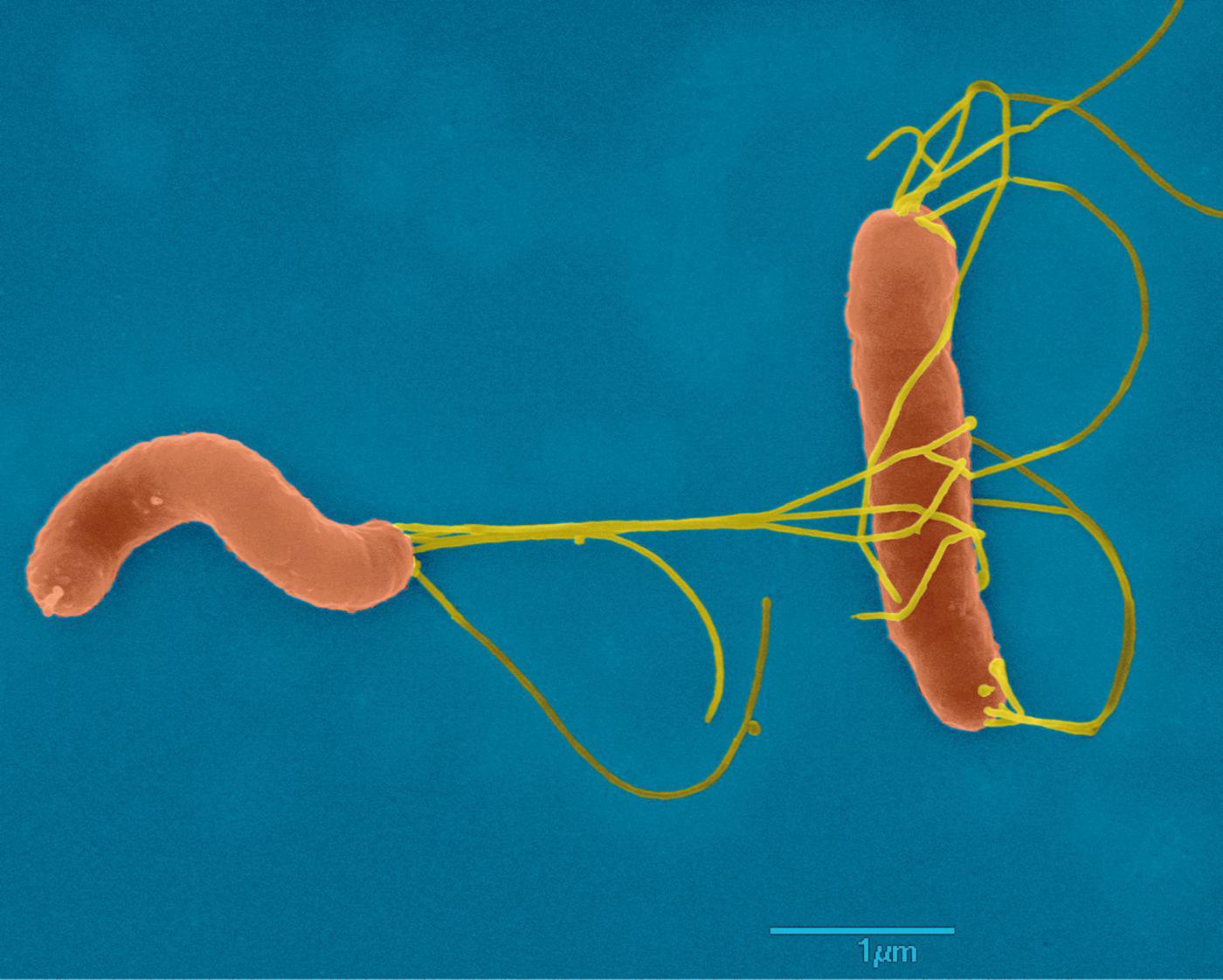
« Helicobacter pylori est la seule bactérie capable de se multiplier dans les conditions d’acidité de l’estomac. Elle infecte 50% de la population mondiale, à risque d’ulcères gastro-duodénaux, de gastrites chroniques, et, dans 1 à 3% des cas, de cancers de l’estomac », indique Hilde De Reuse, responsable de l’unité de Pathogenèse de Helicobacter à l’Institut Pasteur. « Nous cherchons à comprendre les mécanismes moléculaires qui permettent à Helicobacter pylori de survivre dans l’environnement hostile de l’estomac, et de s’y maintenir des années en y provoquant des lésions. En décryptant ces mécanismes, nous avons trouvé de nouvelles cibles thérapeutiques, notamment un transporteur de nickel indispensable à l’activité de l’uréase, une enzyme essentielle à la bactérie pour coloniser l’estomac. » Découvrir des cibles pour de futurs médicaments est aujourd’hui crucial car si un traitement à base d’antibiotiques permet d’éradiquer la bactérie chez la majorité des personnes infectées, son efficacité est grandement menacée par l’antibiorésistance croissante de H. pylori.
Dans le même laboratoire, d’autres avancées laissent espérer un diagnostic précoce du cancer de l’estomac, responsable de 800 000 morts par an dans le monde. « Nous étudions les facteurs de l’hôte associés à la pathogenèse de l’infection », explique Eliette Touati. « Grâce à des collaborations dans le Réseau international des instituts Pasteur, nous avons pu analyser un grand nombre de patients atteints de gastrites et de cancers de l'estomac. Nous avons ainsi identifié deux "biomarqueurs" potentiels, détectables dans le sang. Notre objectif vise à combiner plusieurs biomarqueurs qui signeraient une phase très précoce du cancer de l’estomac, pour pouvoir identifier les personnes à risque. » Ceci permettrait de les traiter précocément par antibiotiques pour éradiquer l’infection par H. pylori et espérer ainsi stopper l’évolution du cancer, mais aussi d’augmenter les chances de guérison des patients ayant déjà des lésions cancéreuses.