Trouver sa voie, donner du sens à ses choix et oser entreprendre. Voilà ce que Caroline Demangel a su forger au fil de sa carrière. Dans ce milieu exigeant et compétitif de la science, elle a su faire confiance à ses aspirations et accepter les nouveaux défis. En 2021, cette chercheuse et son équipe ont révélé une nouvelle cible thérapeutique contre le cancer de la moelle osseuse.
« L’important, ce n’est pas la destination, mais le voyage en lui-même » disait Robert Louis Stevenson. Pour Caroline Demangel, le chemin parcouru lui a permis de choisir sa voie et de diriger sa propre équipe. Concernant la destination, elle ne perd jamais de vue que ses recherches puissent contribuer, si possible, à améliorer la santé humaine.
Trouver sa voie, donner du sens à ses choix
Dès son plus jeune âge, coachée par sa grand-mère institutrice, Caroline se révèle être une élève brillante ; elle saute deux classes au cours de sa scolarité. Plus tard, elle intègre la prestigieuse école d’agronomie aujourd’hui appelée AgroParisTech. Elle réalise alors que l’ingénierie des productions végétales et animales n’est pas ce qu’elle souhaite étudier, et oriente son cursus vers la santé humaine. Après une spécialisation en biochimie elle entreprend une thèse sur la modélisation de la croissance cellulaire et de la production d’anticorps des hybridomes, en parallèle de son emploi d’ingénieure chez Bertin technologies.
Découverte de la recherche académique et d’un continent lointain
En 1993, elle décide d’abandonner le secteur de l’ingénierie et rejoint l’Hybridolab dirigé par Jean-Claude Mazié à l’Institut Pasteur en tant que stagiaire, où elle s’initie aux techniques alors émergentes de criblage de banques d’anticorps recombinants à chaîne unique.
Cette incursion en laboratoire confirme son envie de poursuivre son parcours scientifique en recherche académique. Pour réaliser ses ambitions, elle postule et obtient une bourse post-doctorale de l'Institut Pasteur, puis un poste de chargée de recherche, et décide de compléter sa formation avec un deuxième post-doctorat.
En 1995, départ pour l’Australie avec ses deux très jeunes enfants. Son conjoint adhère à ce projet et la soutient. Il quitte son poste de consultant en région parisienne.

Outre la découverte de ce continent étonnant et la qualité de vie à Sydney, cette expérience a été l’opportunité de bâtir un nouveau projet de recherche, et d’approfondir mes connaissances en immunologie.
Elle rejoint le groupe de recherche sur les mycobactéries, dirigé par Warwick Britton au Centenary Institute de Sydney, pour concevoir et tester des vaccins anti-tuberculeux innovants, ciblant les cellules dendritiques grâce à des anticorps à chaîne unique.
En 2002, forte de ces nouveaux acquis, retour à Paris dans l’unité de Génétique moléculaire bactérienne dirigée par Stewart Cole (qui sera lui-même nommé directeur général de l’Institut Pasteur en 2017). Elle y contribuera à l’évaluation de mycobactéries modifiées comme vaccins anti-tuberculeux, et y développera une nouvelle aire d’expertise autour d’une mycobactériose tropicale négligée : l’ulcère de Buruli.
Créer son unité, mener ses propres projets
Caroline a postulé et obtenu la création de sa propre unité en 2011.
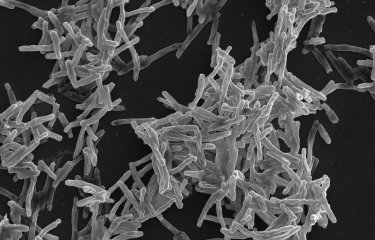
Aujourd’hui son laboratoire ‘Immunobiologie et Thérapie’ constitué de 12 personnes vise à découvrir de nouvelles stratégies pour stimuler ou neutraliser le système immunitaire. Il s’inspire des agents responsables de l’ulcère de Buruli et de la tuberculose, Mycobacterium ulcerans et Mycobacterium tuberculosis, car ces bactéries ont trouvé le moyen de s’installer à long terme dans l’organisme en échappant à notre immunité.

Nous étudions les interactions entre ces pathogènes et notre système immunitaire pour identifier les mécanismes d’attaque et de défense mis en jeu de part et d’autre, et éventuellement les exploiter.
Au-delà des mycobactérioses, comprendre et manipuler le système immunitaire a en effet de multiples applications potentielles. "Lors d’une greffe, il est important d’inhiber les réponses immunitaires, pour éviter un rejet. A l’inverse il est utile de pouvoir les potentialiser lors d’une infection ou d’un cancer."
De la découverte fondamentale à la start-up
C’est en étudiant l’ulcère de Buruli que le laboratoire a découvert en 2021 une nouvelle cible thérapeutique en Oncologie.
M. ulcerans produit une molécule naturelle originale (la mycolactone) qui provoque la mort cellulaire au site d’infection. L’équipe a identifié la cible de la mycolactone dans nos cellules, un complexe protéique appelé ‘translocon’, et émis l’idée qu’il pourrait représenter un nouvel angle d’attaque des cellules cancéreuses. Un partenariat avec l’hôpital Saint Louis de Paris validera le concept que bloquer le translocon est efficace pour tuer sélectivement les cellules de myélome multiple. Ce cancer de la moelle osseuse, encore incurable, touche plus de 5000 nouvelles personnes chaque année en France.

La mycolactone nous a permis de révéler un levier d’action thérapeutique inédit. Nous cherchons aujourd’hui à développer des candidats médicaments qui exploitent ce mécanisme. La signature d’un partenariat avec des investisseurs en 2022 nous donne les moyens de tenter cette nouvelle aventure .
Trouver de nouvelles pistes d’intervention contre la tuberculose, un défi majeur
Mais les projets ne manquent pas, Caroline Demangel souhaite également poursuivre ses recherches sur la tuberculose.
« La tuberculose reste une maladie infectieuse de première importance au niveau mondial, avec plus que 10 millions de cas, entraînant 1,4 millions de morts chaque année.
Des milliards de personnes sont infectées de manière latente. En vieillissant leur immunité diminue, les bacilles peuvent se réactiver, proliférer …même 40 ans plus tard ! »
Le B.C.G. (Bacille de Calmette et Guérin) est le seul vaccin licencié actuellement pour lutter contre la tuberculose. Ce vaccin qui a fêté son 100e anniversaire en 2021 est néanmoins partiellement efficace : bien qu’il soit très utile pour prévenir les formes graves de la maladie chez les jeunes enfants (près de 90 % d’efficacité dans le cas de méningites tuberculeuses), il protège peu contre les cas de tuberculoses pulmonaires chez les adolescents et adultes. Il ne permet donc pas d’empêcher la transmission de la maladie et d’enrayer l’épidémie mondiale.
Des souches multirésistantes apparaissent à travers le monde et contribuent à aggraver l’impact de cette maladie.
Avec ses collaborateurs Albert Pol et Robert G. Parton, Caroline a reçu cette année un prestigieux financement du Conseil européen de la recherche (ERC) pour étudier comment les gouttelettes lipidiques, ces organites stockant les lipides dans nos cellules, contribuent à lutter contre les infections microbiennes. Jusqu’ici, les gouttelettes lipidiques étaient considérées comme de simples réservoirs d’énergie alimentant la croissance des microbes envahisseurs. Mais des études récentes ont conduit à les considérer comme des lanceuses d’alerte, capables de déclencher et organiser des réponses immunitaires contre les pathogènes intracellulaires. Le projet financé par l'ERC déploiera un large éventail de techniques de pointe pour caractériser les mécanismes moléculaires sous-jacents, et ouvrira ainsi la voie à de nouvelles approches anti-infectieuses, notamment antituberculeuses.
|