Une collaboration internationale constituée par des chercheurs de l’Institut Pasteur du Cambodge, de l’Institut Pasteur à Paris, et du National Institutes of Health (NIH), a permis la mise au point du premier test in vitro adapté à la réalité du terrain pour étudier la résistance de Plasmodium falciparum (parasite responsable du paludisme sévère) aux dérivés de l’artémisinine, un constituant majeur des traitements antipaludiques actuellement utilisés. Ce test a vocation à être largement diffusé afin de faciliter la surveillance de la résistance parasitaire aux antipaludiques. Il constitue également un outil de choix pour étudier les bases biochimiques et moléculaires de la résistance aux dérivés de l’artémisinine.
Communiqué de presse
Paris, le 11 septembre 2013
Prévenir la diffusion des parasites résistants à la dernière génération d’antipaludiques que sont les dérivés de l’artémisinine nécessite leur détection rapide par des outils performants. Compte tenu des méthodes disponibles, ceci était inenvisageable jusqu'à présent. En effet, seules des études cliniques coûteuses et contraignantes pour les malades permettaient de détecter ces résistances. Cependant, un test mis au point grâce à des travaux menés par l’unité d’Epidémiologie moléculaire du paludisme, à l’Institut Pasteur du Cambodge, en collaboration avec des équipes de l’Institut Pasteur à Paris et du NIH, vient changer la donne.
Les chercheurs de l'Institut Pasteur et du NIH ont mis au point un test qui permet d’étudier les formes résistantes du paludisme aux dérivés de l’artémisinine. Facile à mettre en œuvre, ce test est adapté à la réalité du terrain et donc diffusable à grande échelle à des fins de surveillance. Son fonctionnement est le suivant : un unique prélèvement sanguin est effectué chez un patient atteint du paludisme. Les parasites présents dans le sang sont ensuite cultivés en présence d’une forte dose d’antipaludique pendant quelques heures. Le degré de résistance est évalué après 3 jours et défini par le nombre de parasites ayant survécu à l’exposition de l’antipaludique. Plus ce nombre est élevé, plus le parasite est résistant au traitement.
Une autre version du test, applicable dans les laboratoires de recherche a également été mise au point. Elle ouvre des perspectives intéressantes en permettant l’étude fine des mécanismes biologiques mis en place par le parasite pour résister aux traitements, ainsi que la recherche de nouvelles molécules actives contre les parasites résistants aux dérivés de l’artémisinine. Dans leur étude, les chercheurs indiquent que les précédents essais de mise au point étaient jusqu’à présent infructueux en raison de l’utilisation de concentrations d’antipaludiques bien inférieures à celles rencontrées par le parasite chez un patient traité.
Grâce à leur test, les auteurs ont également pu déterminer pour la première fois à quel stade de son développement le parasite Plasmodium falciparum résiste aux dérivés de l’artémisinine. Ainsi, ce sont les formes jeunes du parasite qui sont responsables de la perte d’efficacité du traitement.
Compte tenu de sa facilité d’utilisation et de son intérêt dans la lutte contre le paludisme, le test mis au point conjointement par des équipes de l’Institut Pasteur du Cambodge, de l’Institut Pasteur à Paris, et du NIH, a vocation à être diffusé dans les zones d’endémie. Il sera dans un premier temps rapidement étendu au continent asiatique avec pour objectif principal l’établissement d’un réseau de surveillance capable de définir précisément les zones géographiques où les parasites résistants sont présents afin d’adapter les traitements, et prévenir leur diffusion à d’autres zones d’endémie.
--
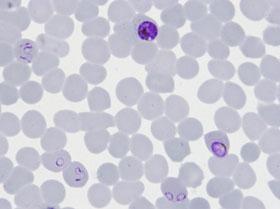
Illustration - Copyright Institut Pasteur
Légende - Frottis sanguin révélant par microscopie la présence du parasite Plasmodium falciparum (en violet) à l'intérieur d'hématies humaines.
Source
Novel phenotypic assays for the detection of artemisinin-resistant Plasmodium falciparum malaria in Cambodia: in-vitro and ex-vivo drug-response studies, The Lancet Infectious Diseases, September 11.
Benoit Witkowski (1), Chanaki Amaratunga (2), Nimol Khim (1), Sokunthea Sreng (3), Pheaktra Chim (1), Saorin Kim (1), Pharath Lim (1,2,3), Sivanna Mao (4), Chantha Sopha (5), Baramey Sam (6), Jennifer M. Anderson (2), Socheat Duong (3), Char Meng Chuor (3), Walter R. J. Taylor (7), Seila Suon (3), Odile Mercereau-Puijalon (8), Rick M. Fairhurst (2), Didier Menard (1).
(1) Malaria Molecular Epidemiology Unit, Institut Pasteur du Cambodge, Phnom Penh, Cambodia ;
(2) Laboratory of Malaria and Vector Research, National Institute of Allergy and Infectious Diseases,
National Institutes of Health, Bethesda, MD, USA ;
(3) National Center for Parasitology, Entomology and Malaria Control, Phnom Penh, Cambodia ;
(4) Sampov Meas Referral Hospital, Pursat, Cambodia ;
(5) Makara 16 Referral Hospital, Preah Vihear, Cambodia ;
(6) Ratanakiri Referral Hospital, Ratanakiri, Cambodia ;
(7) Service de Médecine Internationale et Humanitaire, Hôpitaux Universitaires de Genève, Geneva ;
(8) Parasite Molecular Immunology Unit, Institute Pasteur, Paris, France.
Contact
Service de presse de l’Institut Pasteur
Jérémy Lescène - Jeremy.lescene@pasteur.fr - +33 (0)1 45 68 81 01
Nadine Peyrolo - nadine.peyrolo@pasteur.fr - +33 (0)1 45 68 81 47