Françoise Barré-Sinoussi est rétrovirologiste, prix Nobel de médecine en 2008 pour la découverte du virus du sida (avec Luc Montagnier), et présidente de l’association Sidaction depuis novembre 2017. Elle a été récompensée par l’Institut Pasteur pour son travail sur le virus VIH1, en proposant sa nomination en tant que membre de la National Academy of Inventors* aux Etats-Unis. Alors que l’Institut Pasteur est dans sa 130e année d’existence - 130 ans célébrés le 14 novembre 2018 – nous avons rencontré la lauréate pour l’interroger sur sa découverte et la recherche sur le sida.
*Adhérant de la National Academy of Inventors (NAI) aux Etats-Unis, depuis 2015, l’Institut Pasteur a souhaité célébrer la curiosité, la créativité, l’innovation, l’invention et la richesse de la culture pasteurienne. Le 27 juin 2017, l’Institut a ainsi récompensé 14 de ses inventeurs qui ont été nommés membres de la NAI. L’événement a fait résonner l’esprit pionnier de Louis Pasteur et de celui des générations de chercheurs pasteuriens qui se sont succédé. Les travaux de recherche de ces 14 scientifiques mis à l’honneur ont donné lieu à plusieurs brevets américains ayant fait l’objet d’une exploitation de licences ayant un impact positif pour la société et pour l’Institut.

Pouvez-vous nous dire quelques mots de la découverte du virus du sida, VIH1, en 1983 ?
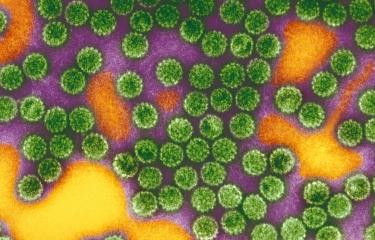
La première détection du virus par mesure d’une activité enzymatique rétrovirale, la transcriptase inverse, dans une culture de cellules ganglionnaires d’un patient date de janvier 1983. Elle a été suivie par l’observation du virus, par Charles Dauguet, le « microscopiste » du laboratoire en février 1983. Ce travail fût publié dans la revue Science, en mai 1983. Puis nous avons étudié les principales caractéristiques de ce nouveau rétrovirus humain, appelé alors Lymphadenopathy Associated Virus (ou LAV) et démontré qu’il était responsable du sida.
L’isolement du virus VIH-1 en 1983 a été une découverte fondamentale, le point de départ d’intenses recherches internationales pour lutter contre l’infection et elle a notamment permis très rapidement de mettre au point des tests de diagnostic de l’infection VIH. Ce sont ces inventions-là, utiles aux patients, que l’Institut Pasteur a souhaité saluer rétrospectivement en 2017. Car, en les récompensant, l’Institut rend hommage à la vision globale de Louis Pasteur, toujours d’actualité : une recherche scientifique multidisciplinaire au bénéfice de la santé humaine.
Quel regard portez-vous sur plus de 30 ans de recherche biomédicale sur le VIH/sida ?
C’est le plus bel exemple existant d’un parallélisme complet entre des avancées de la recherche et leurs applications en santé publique. En premier lieu, la découverte du virus a permis de disposer dès 1985 des premiers tests de diagnostic. Puis le traitement a dérivé de la connaissance du virus, de son mode de réplication dans les cellules cibles, etc. Il y eut la première molécule montrant une certaine efficacité, l’AZT, en 1985, puis les traitements actuels en 1996, une combinaison d’au moins trois molécules permettant une espérance de vie similaire à celle de personne non infectée. La première démonstration que ce traitement est aussi efficace pour prévenir l’infection date de 1994 avec les résultats sur la prévention la transmission mère-enfant par l’AZT. Depuis 2011, on sait qu’un patient sous antirétroviraux ayant une infection parfaitement bien contrôlée ne transmet plus le virus aux autres. De plus, ces molécules antirétrovirales sont également efficaces en prophylaxie pré-exposition (PreP). Enfin, grâce à la connaissance du génome du virus, des outils pour mesurer la charge virale, évaluer la résistance aux médicaments, et donc modifier le traitement d’un patient en cas d’échec thérapeutique, ont pu être élaborés.
L’Institut Pasteur a participé à l’étude ANRS VISCONTI, il y a quelques années, qui a marqué un tournant. Elle a fait état de 14 patients ayant pu arrêter leur traitement. De quoi s’agit-il ?
Ce sont des patients qui ont été traités très précocement, environ 10 semaines après le début de l’infection. Au bout de 3 ans, ils avaient une charge virale indétectable et ils ont souhaité une interruption thérapeutique. Sans traitement depuis plusieurs années, ils ont toujours une charge virale indétectable, et un niveau extrêmement bas de réservoirs viraux – cellules où le virus reste à l’état latent et se réactive à l’arrêt du traitement. Le traitement précoce a donc limité l’établissement des réservoirs et la propagation du virus. Un réseau d’équipes françaises étudie ces patients pour comprendre les mécanismes précis de ce contrôle particulièrement efficace.
Pourra-t-on guérir un jour du sida ?
Je ne sais pas dans combien de temps nous pourrons parler de guérison du sida, mais si nous ne tentons rien, nous ne l’aurons jamais ! Je ne suis pas sûre personnellement que nous parvenions à la guérison complète avec élimination du virus de tous les compartiments de l’organisme, mais je suis persuadée que nous réussirons à obtenir la “rémission durable” qui permettra aux patients d’arrêter leur traitement et de maintenir le virus sous contrôle et donc, non transmissible, à l’image des patients VISCONTI. L’initiative que j’ai lancé en 2011, avec la Société internationale sur le sida, a permis de créer une alliance internationale afin d’accélérer la recherche de ces nouvelles stratégies thérapeutiques du futur.
Les recherches sur le VIH peuvent-elles avoir des retombées sur d’autres maladies ?
Oui, et elles en ont déjà ! L’étude du VIH/sida a d’ores et déjà fait avancer l’immunologie, avec une meilleure connaissance des acteurs de notre défense immunitaire, qui bénéficie à diverses recherches biomédicales. Et l’infection par le VIH partage par exemple un élément commun, l’inflammation, avec de nombreuses maladies : cancers, maladie d’Alzheimer, maladies du vieillissement, diabète… C’est pourquoi les chercheurs dans le domaine du VIH et les experts d’autres pathologies doivent interagir pour espérer de nouveaux progrès contre le sida et d’autres maladies. Nous avons beaucoup à apprendre les uns des autres.
HISTOIRE - La découverte du VIH-1
Au début des années 80, à l’Institut Pasteur…
- 21 septembre 1982 : un an après la description aux Etats-Unis d’un nouveau syndrome d’immunodéficience inexpliqué, les premiers cas sont remarqués en France. Willy Rozenbaum, clinicien parisien, pense qu’il s’agit d’un nouveau virus humain, peut-être un “rétrovirus”.
Alors qu’il donne une conférence à l’Hôpital Pasteur, il espère convaincre des chercheurs de l’Institut Pasteur de travailler avec lui sur cette infection d’origine inconnue, mais seuls des médecins sont dans la salle. Sa collègue Françoise Brun-Vezinet, médecin-virologue, lui suggère alors de contacter les enseignants du cours de rétrovirologie qu’elle a suivi à l’Institut Pasteur : Jean-Claude Chermann et Luc Montagnier. Ce dernier, chef de l’unité d’Oncologie virale, axée sur les relations rétrovirus-cancers, accepte d’aider Willy Rozenbaum et propose à Jean-Claude Chermann et à une chercheuse de son groupe, Françoise Barré-Sinoussi, de s’impliquer dans cette recherche. - Décembre 1982 : une première réunion entre cliniciens et chercheurs a lieu à l’Institut Pasteur et permet de définir une stratégie de recherche en fonction des observations cliniques faites chez les patients.
- Janvier 1983 : L’équipe pasteurienne reçoit le premier ganglion d’un patient au stade “pré-sida” (avant l’apparition d’une immunodéficience profonde). Il fallait que les cellules cibles du virus soient encore présentes pour espérer l’isoler, or à un stade plus avancé de la maladie, le taux de lymphocytes CD4 tombait en flèche jusqu’à disparaître quasi complètement. Les cellules ganglionnaires sont mises en culture et l’équipe recherche régulièrement la présence de rétrovirus par la détection de l’activité d’une enzyme typique de cette famille virale (la transcriptase réverse).
- Trois semaines plus tard : l’activité enzymatique est détectée, mais un phénomène de mort cellulaire est observé de façon concomitante. Moment d’inquiétude pour les chercheurs : ils risquent de perdre immédiatement le virus qui vient pour la première fois d’être détecté. L’équipe pasteurienne décide en urgence d’ajouter immédiatement dans la culture des globules blancs de donneurs de sang : l’activité enzymatique rétrovirale est à nouveau détectée…
- 4 février 1983, 17h45. Le “microscopiste” de l’unité, Charlie Dauguet, se voit confier la tâche délicate de visualiser au microscope électronique des particules de type rétrovirus dans la culture. Après beaucoup de patience, le 4 février 1983, à 17h45, il hurle : « Eurêka, ça y est, je le vois, je l’ai ! ». L’équipe teste ensuite les cultures avec les réactifs correspondant au seul rétrovirus humain connu à l’époque, le HTLV, décrit aux États-Unis en 1980 par le Pr Gallo. Les tests sont négatifs. L’équipe pasteurienne a bien découvert un tout nouveau rétrovirus.
La première photo du virus du sida, en 1983.